Química Orgánica- 2025
Sección fuera de línea
-
-
-
1.2 MB · Subido 13/08/2025 14:41
-
610.9 KB · Subido 19/08/2025 16:47
-
La química orgánica es la química de los compuestos del carbono.
El nombre engañoso “orgánico” es una reliquia de los tiempos en que los compuestos químicos se dividían en dos clases: inorgánicos y orgánicos, según de dónde provenían. Los compuestos inorgánicos eran aquellos que provenían de los minerales y los orgánicos los que se obtenían de fuentes vegetales y animales, o sea: de materiales producidos por organismos vivos. Hace años, los químicos pasaban mucho tiempo haciendo extracciones, purificando y analizando las sustancias provenientes de animales y plantas. Se sentían motivados por su curiosidad natural con respecto a la materia viva, así como por el deseo de obtener, a partir de la naturaleza, ingredientes para las medicinas, colorantes y otros productos de utilidad. Los científicos pensaban que los compuestos que se encuentran en la materia viva eran diferentes de las otras sustancias y que contenían una fuerza vital intangible que les daba vida. Esta idea hizo que los químicos no trataran de obtener compuestos orgánicos en el laboratorio.
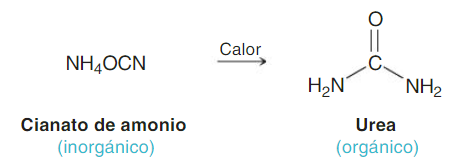 Sin embargo, en 1828 el químico alemán Friedrich Wöhler, que tenía entonces 28 años, accidentalmente preparó urea (que, como es sabido, es un constituyente de la orina) al calentar cianato de amonio, una sustancia inorgánica (o mineral). Este experimento y otros parecidos desacreditaron poco a poco la teoría de la fuerza vital y abrieron el camino para la moderna química orgánica sintética.
Sin embargo, en 1828 el químico alemán Friedrich Wöhler, que tenía entonces 28 años, accidentalmente preparó urea (que, como es sabido, es un constituyente de la orina) al calentar cianato de amonio, una sustancia inorgánica (o mineral). Este experimento y otros parecidos desacreditaron poco a poco la teoría de la fuerza vital y abrieron el camino para la moderna química orgánica sintética.Los compuestos de fuentes orgánicas tenían esto en común: todos contenían el elemento carbono. Aún después de que quedó establecido que estos compuestos no necesariamente debían provenir de fuentes vivas, ya que podían hacerse en el laboratorio, resultó conveniente mantener el nombre orgánico para describirlos, así como también compuestos similares, reteniéndose hasta la fecha esta división entre compuestos inorgánicos y orgánicos.
Aunque aún hoy muchos compuestos del carbono se aíslan más convenientemente de fuentes vegetales y animales, la mayoría de ellos se obtienen por síntesis (la síntesis consiste en ir uniendo moléculas pequeñas y relativamente sencillas, para formar otras más grandes y complejas). A veces, se sintetizan de sustancias inorgánicas, tales como carbonatos y cianuros, pero más a menudo se parte de otros compuestos orgánicos.

 Hay dos grandes fuentes de las que se pueden obtener sustancias orgánicas simples: el petróleo y el carbón (ambas son orgánicas en el sentido tradicional, puesto que son producto de la descomposición de plantas y animales). Estas sustancias simples se emplean como elementos constructivos, a partir de los cuales se pueden hacer compuestos más complicados. Algunos ejemplos de sustancias que inicialmente se aislaron de la naturaleza pero que actualmente se producen sintéticamente para su uso comercial son las vitaminas, los aminoácidos, el colorante índigo, el alcanfor, que es un repelente de polillas y el antibiótico penicilina. La mayoría de los fármacos que se utilizan en medicina son sintéticos (incluyendo la aspirina, el éter, la novocaína y los barbituratos). A pesar de que algunas veces el término sintético se ve con recelo, como si conllevara algo artificial o no natural, los productos naturales sintéticos antes mencionados son, de hecho, idénticos a los compuestos que se extraen de fuentes naturales.
Hay dos grandes fuentes de las que se pueden obtener sustancias orgánicas simples: el petróleo y el carbón (ambas son orgánicas en el sentido tradicional, puesto que son producto de la descomposición de plantas y animales). Estas sustancias simples se emplean como elementos constructivos, a partir de los cuales se pueden hacer compuestos más complicados. Algunos ejemplos de sustancias que inicialmente se aislaron de la naturaleza pero que actualmente se producen sintéticamente para su uso comercial son las vitaminas, los aminoácidos, el colorante índigo, el alcanfor, que es un repelente de polillas y el antibiótico penicilina. La mayoría de los fármacos que se utilizan en medicina son sintéticos (incluyendo la aspirina, el éter, la novocaína y los barbituratos). A pesar de que algunas veces el término sintético se ve con recelo, como si conllevara algo artificial o no natural, los productos naturales sintéticos antes mencionados son, de hecho, idénticos a los compuestos que se extraen de fuentes naturales.¿Qué tienen en especial los compuestos del carbono que justifiquen su separación de los de todos los demás cientos y tantos elementos del Sistema Periódico? Parcialmente, al menos, la respuesta parece ser esta: hay muchísimos compuestos del carbono y sus moléculas pueden ser muy grandes y complejas.
El número de compuestos que contienen carbono es varias veces mayor que el número de sustancias que no lo contienen. Se conocen moléculas orgánicas que contienen miles de átomos, cuyo arreglo puede ser muy complicado, aún en moléculas relativamente pequeñas.
¿Qué propiedad tan especial posee el carbono como para permitirle formar tantos compuestos? Los átomos de carbono pueden unirse entre sí hasta un grado que es imposible para átomos de cualquier otro elemento. Pueden formar cadenas de miles de átomos o anillos de todos los tamaños: estas cadenas y anillos pueden tener ramificaciones y uniones cruzadas- A los carbonos de estas cadenas y anillos se unen otros átomos: principalmente hidrógeno y además también flúor, cloro, bromo, yodo, oxígeno, nitrógeno, azufre, fósforo y muchos otros.
Cada arreglo atómico diferente corresponde a un compuesto distinto y cada compuesto tiene su conjunto de características químicas y físicas. No es sorprendente que hoy se conozcan 16 millones de compuestos del carbono y que se conozcan miles más cada año. No es sorprendente que el estudio de su química sea un campo especializado.
La química orgánica está presente en la vida diaria. Estamos formados y rodeados por compuestos orgánicos. Casi todas las reacciones de la materia viva involucran compuestos orgánicos: es imposible comprender la vida, al menos desde el punto de vista físico, sin saber algo sobre química orgánica. Los constituyentes principales de la materia viva –proteínas, carbohidratos, lípidos (grasas), ácidos nucleicos (DNA, RNA), las membranas celulares, enzimas, hormonas- son orgánicos.
Otras sustancias orgánicas incluyen la gasolina, aceites, las llantas de los automóviles, la ropa que utilizamos, la madera de nuestros muebles, el papel de nuestros libros, las medicinas que tomamos, los recipientes de plástico, las películas para fotografía, los perfumes, las alfombras y las telas. Diariamente, se hace referencia al polietileno, a resinas epóxicas, Estirofoam, nicotina, grasas poliinsaturadas y colesterol: todos estos términos se refieren a sustancias orgánicas.
En pocas palabras, la química orgánica es mucho más que una rama de la ciencia: es parte de nuestra cultura tecnológica.
-
Antes de comenzar el desarrollo de la asignatura es conveniente ver algunos conceptos:
1. Los compuestos orgánicos son aquellos en cuya composición interviene el carbono.
2. La composición de un compuesto está dada por la fórmula molecular.
3. La constitución de un compuesto, es decir, su fórmula estructural o estructura, da el orden en que los átomos presentes en la molécula están unidos entre sí.
Ejemplo:

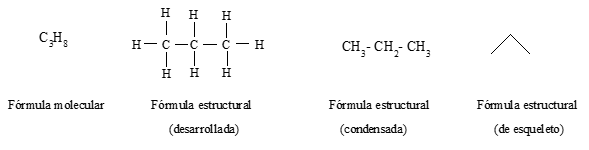
La fórmula estructural desarrollada indica todos los enlaces presentes en la molécula.
En la fórmula estructural condensada no se desarrollan los enlaces entre atomos de carbono y de hidrógeno.
En la fórmula de esqueleto, cada línea indica los átomos de carbono enlazados, dándose por sobreentendido que los átomos de carbono están unidos a todos los átomos de hidrógeno correspondientes.
4. El átomo de carbono puede formar hasta cuatro enlaces covalentes.
5. El átomo de carbono puede constituir cadenas, que pueden ser:
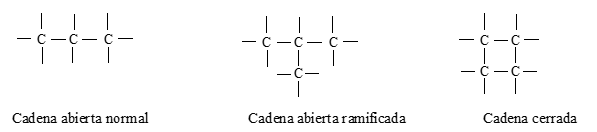
- Cadenas abiertas (acíclicas) o cerradas (cíclicas).
- Cadenas normales (lineales) o ramificadas.
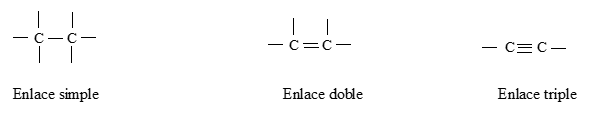
 6. Los átomos de carbono pueden unirse entre sí, formando enlaces (uniones o ligaduras), que pueden ser:
6. Los átomos de carbono pueden unirse entre sí, formando enlaces (uniones o ligaduras), que pueden ser:- Enlaces simples
- Enlaces dobles
- Enlaces triples

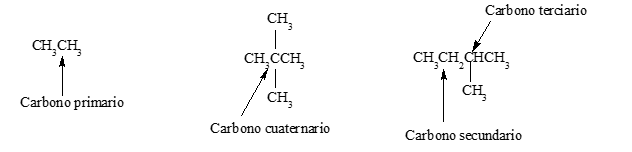
7. El átomo de carbono de una cadena puede ser primario, secundario, terciario o cuaternario según el número de carbonos a los que se une.
 8. Se define grupo funcional como un grupo de átomos o conjunto de átomos que le otorgan a la molécula propiedades y reactividad característica.
8. Se define grupo funcional como un grupo de átomos o conjunto de átomos que le otorgan a la molécula propiedades y reactividad característica.9. Se denomina serie homóloga al conjunto de compuestos que tienen el mismo grupo funcional, pero difieren en el número de átomos de carbono de sus moléculas, más específicamente en el número de unidades —CH2. Por ejemplo, la siguiente es una serie homóloga de hidrocarburos: CH3—CH3, CH3—CH2—CH3, CH3—CH2—CH2—CH3.
En una molécula orgánica se puede distinguir una parte hidrocarbonada (formada por los enlaces C-H y C-C) que puede influir en las características físicas y químicas pero que, finalmente, quedan fuertemente determinadas por la otra parte de la molécula que comprende los grupos funcionales.
Se indican a continuación los principales grupos funcionales.
Serie homóloga
Grupo funcional
Alcanos
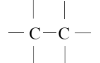


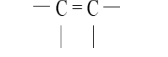
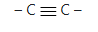
Haluros de alquilo
- X
X (halógeno) unido a carbono alifático
Haluros de arilo
– X
X (halógeno) unido a carbono aromático
– OH
OH unido a carbono alifático
Fenoles
– OH
OH unido a carbono aromático
– O –
O unido a carbonos alifáticos y/o aromáticos
Aldehídos
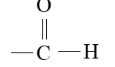

Cetonas

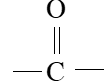
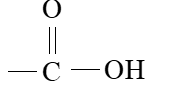

Aminas
– NH2 (primaria)
– NH – (secundaria)
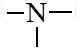

(terciaria)
Ésteres
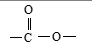

Haluros de acilo
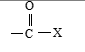

Anhídridos de ácidos
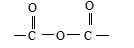

Amidas