ISOMERÍA
3. Isomería espacial o estereoisomería
3.3. Isomería óptica
A principios de siglo XIX el físico Jean-Baptiste Biot señaló que algunas sustancias orgánicas de origen natural poseían la propiedad de girar el plano de la luz polarizada. Este fenómeno consiguió explicarse cuando los químicos comenzaron a considerar la disposición tridimensional de las moléculas en el espacio y la configuración tetraédrica del átomo de carbono
Las propiedades geométricas de un carbono con hibridación sp3 hacen que, en el caso de que esté unido a cuatro átomos o grupos de átomos diferentes, la molécula no tenga plano de simetría y que existan dos maneras diferentes de ordenar a los cuatro átomos o grupos de átomos. Éstas dos configuraciones originan dos formas isoméricas especulares no superponibles llamadas enantiómeros.
El carbono con hibridación sp3 que está unido a cuatro átomos o grupo de átomos diferentes se denomina centro quiral o estereocentro. Cuando se presenta este caso se dice que la molécula es quiral y ópticamente activa, ya que es capaz de desviar el plano de la luz polarizada.
De esta forma, se dice que dos enantiómeros se diferencian por:
- Sus propiedades químicas son idénticas, salvo frente a reactivos ópticamente activos.
- Sus propiedades físicas son iguales, excepto la dirección de rotación del plano de la luz polarizada.
La dirección de rotación de dos enantiómeros es distinta, pero de igual magnitud. Por lo tanto la rotación específica de uno de ellos es (+) y la del otro (-), pero el valor absoluto es igual.
Rotación específica
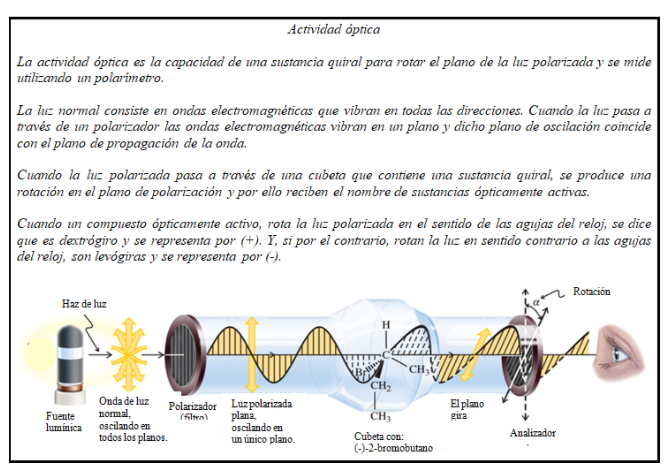
Cuando la luz polarizada plana atraviesa una sustancia quiral, el campo eléctrico interacciona de modo diferente con lo que podríamos llamar mitades “izquierda” y “derecha” de la molécula. Esta diferente interacción da como resultado una rotación del plano de polarización denominada rotación óptica y la muestra que la provoca se dice que es ópticamente activa.
La rotación medida (en grados) en el polarímetro, es la rotación óptica observada, α, de la muestra. Su valor es función de la concentración y de la estructura de la molécula activa, de la longitud de la cubeta que contiene la muestra, de la longitud de la onda de luz incidente, del disolvente y de la temperatura. Con el fin de evitar ambigüedades se ha establecido un valor estándar de α, el cual se conoce como rotación específica, [α] característica de cada compuesto.
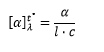
Donde:
[a] = Rotación específica
l = Longitud de onda de la luz incidente; la fuente de luz más común es la correspondiente a la línea D de una lámpara de vapor de sodio (l = 589,3 nm).
T = temperatura en ºC.
a = Rotación observada.
L = Longitud de la cubeta que contiene la muestra, en dm.
c = concentración en gramos por mL de disolución.
Recordar: La rotación específica es una constante física característica de las moléculas ópticamente activas.
Los enantiómeros giran el plano de la luz polarizada el mismo ángulo pero en sentidos opuestos.
Un compuesto que tiene un centro asimétrico (como el 2-bromobutano) puede existir en forma de dos estereoisómeros. Si se imagina un espejo entre los dos estereoisómeros podrá verse que son imágenes especulares entre sí. Además, son imágenes especulares no superponibles y por consiguiente son moléculas diferentes.
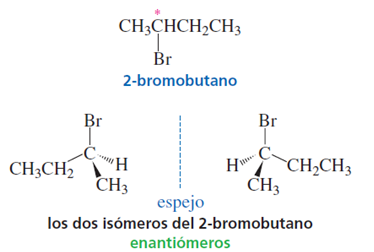
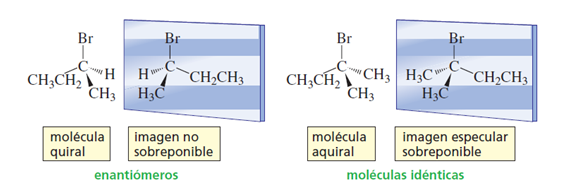
Las moléculas que son imágenes especulares no sobreponible entre sí se llaman enantiómeros (del griego enantion, “opuesto”). Así, los dos estereoisómeros del 2-bromobutano son enantiómeros. Una molécula que tiene imagen especular no sobreponible, como un objeto que tiene imagen especular no sobreponible, es quiral. Por consiguiente, cada miembro de un par de enantiómeros es quiral. Téngase en cuenta que la quiralidad es una propiedad de todo un objeto o de toda una molécula.
Una molécula que tiene una imagen especular sobreponible, como un objeto que tiene una imagen especular sobreponible, es aquiral.
Una mezcla 1:1 de enantiómeros (+) y (-) no presenta rotación óptica y es por lo tanto ópticamente inactiva. Este tipo de mezcla se denomina mezcla racémica.
Los invitamos a visualizar los videos del profesor Ernesto Brunet Romero
Cuando estamos en presencia de distintos estereoisómeros de un compuesto, nos preguntamos cuáles son los nombres que identifican a cada uno de ellos. Para evitar confusiones, es necesario utilizar un sistema de nomenclatura que indique el ordenamiento de los átomos o grupos en torno al centro asimétrico. Por este motivo, en química se emplean las letras R y S. Este sistema fue inventado por R. S. Cahn, C. Ingolg y V. Prelog.
Antes de aplicar esta nomenclatura a un estereocentro, se deben asignar prioridades a los sustituyentes mediante el uso de reglas de secuencia.
Regla 1: Se consideran los átomos directamente unidos al estereocentro. Un sustituyente con mayor número atómico tiene preferencia sobre los de número atómico inferior. Cuando dos sustituyentes tienen idéntica prioridad, se exploran las cadenas de dichos sustituyentes hasta encontrar un punto de diferencia. Los dobles o triples enlaces se tratan como si fueran sencillos, duplicando o triplicando los átomos de la cadena.
Regla 2: Orientar la molécula de modo que el átomo o grupo que tenga la prioridad menor se aleje del espectador. A continuación trazar una flecha imaginaria del grupo o átomo con la mayor prioridad hasta el grupo o átomo con la siguiente prioridad mayor.
1. Si la flecha apunta en el sentido de las manecillas del reloj, el centro asimétrico tiene la configuración R (Rectus en latín: Derecho).
2. Si la flecha apunta en contra del sentido de las manecillas del reloj, el centro tiene una configuración S (Sinister en latín: Izquierdo).
Les dejamos un video del profesor Juan Antonio Llorens Molina. Estereoisomería óptica. Asignación de las configuraciones R/S a los centros quirales
Fórmulasde Fischer
Una proyección de Fischer es una forma simplificada de representar, en dos dimensiones, átomos de carbono tetraédricos y sus sustituyentes. En este método, la molécula se dibuja en forma de cruz, con el átomo central en el punto de intersección. Por convenio, las líneas horizontales representan enlaces dirigidos hacia el observador, y las verticales enlaces que se alejan de éste. Las moléculas en perspectiva deben disponerse de esta forma para facilitar su transformación en proyecciones de Fischer.
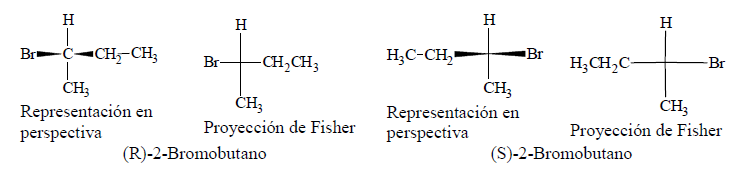
Un ejercicio mental sencillo para transformar representaciones en perspectiva en proyecciones de Fisher es el siguiente:
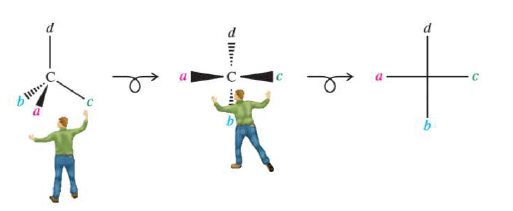
Una vez obtenida la proyección de Fisher, puede interconvertirse en otras equivalentes mediante ciertas rotaciones y permutaciones de sustituyentes. Sin embargo hay que tener mucho cuidado de que tales manipulaciones no alteren la configuración del estereocentro.
Ahora vamos a revisar la manera de determinar la configuración en un compuesto representado como proyección de Fischer.
1. Ordene los grupos que estén enlazados al centro asimétrico por prioridad decreciente.
2. Trace una flecha desde el grupo con la mayor prioridad hasta el grupo con la siguiente prioridad mayor. Si la flecha apunta en el sentido de las manecillas del reloj, el enantiómero presenta configuración R, si apunta en sentido contrario a las aguas del reloj, el enantiómero tiene la configuración S, siempre y cuando el grupo con la menor prioridad esté en un enlace vertical.
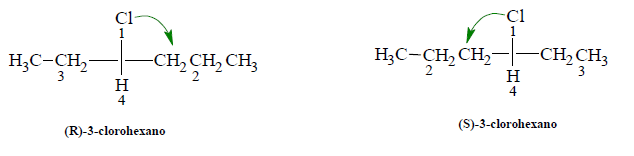
Si el grupo con la menor prioridad está en el enlace horizontal, lo que indica la dirección de la flecha será contrario a lo correcto. En el ejemplo que sigue, el grupo con menor prioridad está en un enlace horizontal, por lo que el sentido de las manecillas indica la configuración S y no la configuración R.

Al trazar la flecha del grupo 1 al grupo 2, se la puede hacer pasar por el grupo con la menor prioridad (4), pero nunca debe dibujarse haciéndola pasar por el grupo con la siguiente prioridad menor (3)

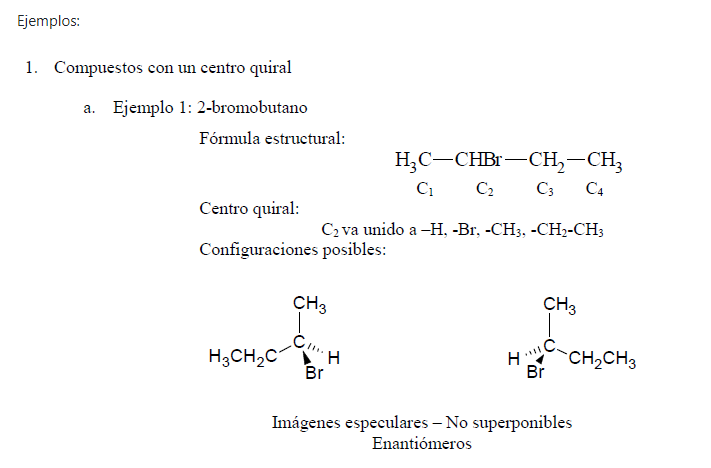
Los enantiómeros giran el plano de la luz polarizada el mismo ángulo pero en sentidos opuestos. Así, para el 2-bromobutano el enantiómero (-) gira el plano 23,1º en sentido antihorario, y su imagen especular (+)-2-bromobutano lo hace 23,1º en sentido horario. De aquí se desprende que una mezcla 1:1 de enantiómeros (+) y (-) no presenta rotación óptica y es por lo tanto ópticamente inactiva. Este tipo de mezcla se denomina mezcla racémica.
2. Compuesto con más de un centro quiral
a. Ejemplo 1: 3-cloro-2-butanol
Muchos compuestos orgánicos tienen más de un centro asimétrico. Cuantos más centros asimétricos tenga un compuesto, más estereoisómeros puede tener. Conociendo el número de centros asimétricos que tiene un compuesto es posible calcular el número máximo de estereoisómeros del mismo:
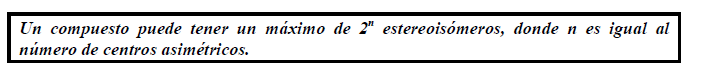
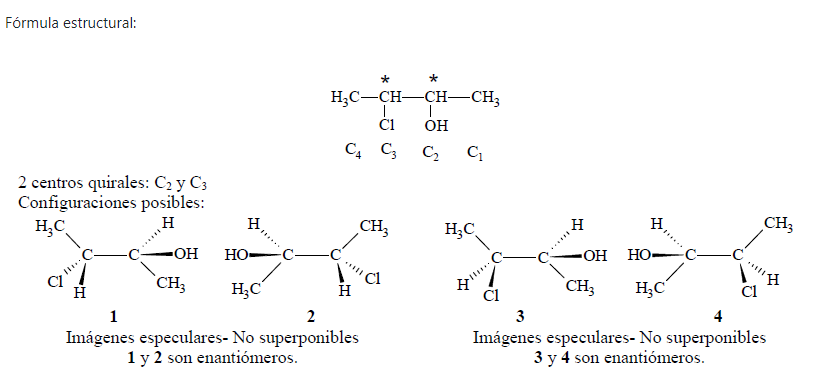
1 y 3 son esteroisómeros que no son idénticos y tampoco son imágenes especulares; se llaman diasterómeros. Los diasterómeros son estereisómeros que NO son enantiómeros. Las configuraciones 1 y 4, 2 y 3, 2 y 4, también son diasterómeros.
Los diasterómeros tienen propiedades físicas distintas (distintos puntos de fusión, de ebullición, solubilidad, rotaciones específicas, entre otras) y distintas propiedades químicas.
Formas meso
Algunos compuestos con dos centros asimétricos tienen solamente 3 estereoisómeros en lugar de 4, es por ello que se dice que el máximo número de estereoisómeros que puede tener un compuesto con n centros asimétricos es 2n.
Un ejemplo de lo anterior es el compuesto 2,3-dibromobutano.
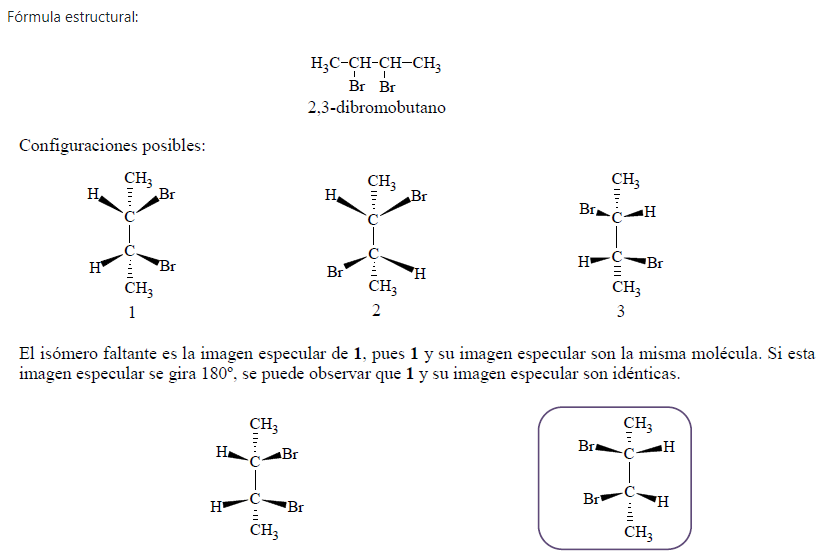
Al estereoisómero 1 se le denomina compuesto meso. El compuesto meso es una molécula aquiral a pesar de contar con centros asimétricos. Esta molécula no provoca giros en el plano de la luz polarizada ya que es superponible con su imagen especular.
Un compuesto meso se reconoce por el hecho de que tiene dos (o más) centros asimétricos y un plano de simetría. Dicho plano corta la molécula por el centro y una mitad es la imagen especular de la otra. El estereoisómero 1 tiene un plano de simetría, por lo tanto no tiene un enantiómero.
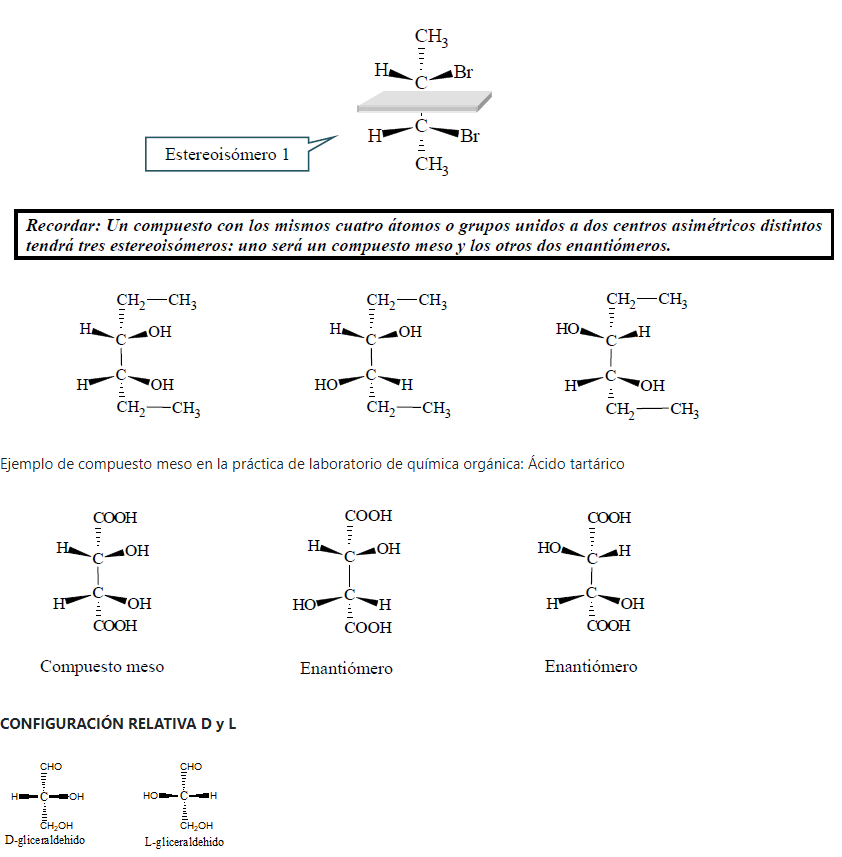
La configuración D-L solamente indica que el compuesto tiene la misma configuración que el D ó L gliceraldehído (con el OH hacia la derecha o hacia la izquierda, respectivamente).
Les dejamos un video del profesor Juan Antonio Llorens Molina. Estereoisómeros ópticos con dos carbonos asimétricos